子宫内膜异位症(EMS)是指有活性的内膜细胞种植在子宫内膜以外的位置,它是一种雌因子依赖的妇科疾病。越来越多的研究发现NCAM1dim FCGR3+ NK细胞和NCAM1bright FCGR3-(一类低杀伤活性、主要分泌细胞因子的)NK细胞比例的失衡和NK细胞杀伤活性不足与多种生理和病理过程相关,包括正常妊娠、传染病、恶性瘤等等,其中也包括子宫内膜异位症。NK细胞杀伤活性不足会导致子宫内膜异位症中局部免疫环境的功能失调,影响异位子宫内膜组织的去除。不过在异位病变微环境(ELM)中NK细胞杀伤活性受损的原因仍不清楚。研究人员正在利用子宫内膜异位症模型探索疾病的预防策略。江苏专业的子宫内膜异位症模型实验外包
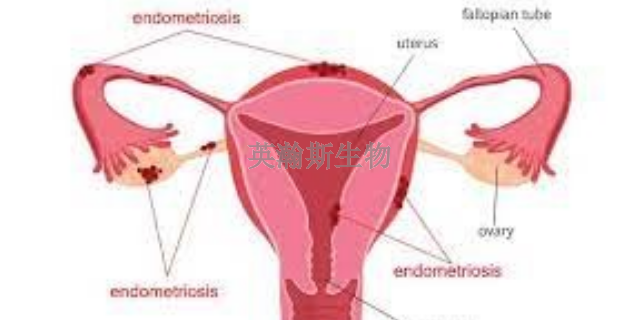
用于子宫内膜异位症的动物模型主要包括以下几种:狲猴、狲狲等非人灵长类动物、家兔、大鼠、小鼠、免疫缺陷小鼠等,其中非人灵长类动物拥有许多与人类相同的特征,类似于人类该病的表现,但此类模型所需经费昂贵;家兔可用于研究EM对卵子释放、拾卵、卵子运送的影响;大鼠与小鼠具有相类似的特点,如性成熟早,繁殖力强,可用于EM对娃振、粘连形成、黄体功能缺陷及自身免疫等方面影响的研究,但Gumming[l]等研究表明小鼠在某些方面可能优于大鼠模型,如环境中的TCDD(二噩英的一种),可抑制小鼠体液免疫TCDD在狲猴模型中经证实可增加EM的发生率;免疫缺陷小鼠可以克服异种间的免疫排斥反应,可保留人子宫内膜组织学、染色体以及生物化学的特性,并且对各种药物的敏感性不发生改变江西大鼠子宫内膜异位症模型有哪家子宫内膜异位症模型的建立为我们提供了一个深入了解疾病的机会。
与正常子宫内膜细胞相比,子宫异位内膜异位症模型细胞的自噬相关基因(MAP1LC3B,也叫LC3B和BECN1,也叫Beclin1)表达水平明显下降。通过将FCGR3- NK细胞分别与抑制自噬(3-MA-ESC和siATG5-ESC)、促进自噬(Rap-ESC)和未处理(Ctrl-ESC)的异位内膜细胞共培养,来模拟体内微环境,结果发现与未处理的ESCs共培养后FCGR3- NK细胞比例上升、而且KIR2DL1和KIR3DL1表达上调、NCR3, NCR2, IFNG, PRF1和GZMB表达下调;而与抑制了自噬的ESCs共培养的NK细胞这种变化更加强烈,与促进自噬的ESCs共培养则会减弱这些变化(Fig2)。
研究人员正在充分利用子宫内膜异位症模型,积极探索疾病的预防策略。他们深知,预防是降低子宫内膜异位症发病率、改善患者生活质量的关键所在。通过模拟疾病的发病环境和过程,研究人员能够更深入地了解疾病的发病机制,从而找到潜在的预防靶点。同时,他们还利用模型对不同的预防方法进行测试,观察其对疾病发生的影响,以期找到比较为有效的预防手段。这一研究不仅有助于我们更好地认识子宫内膜异位症,更能为制定科学的预防策略提供有力支持。相信在不久的将来,随着研究的深入,我们能够找到更为有效的预防方法,为更多女性守护健康。子宫内膜异位症模型的建立有助于推动生殖健康领域的进步。
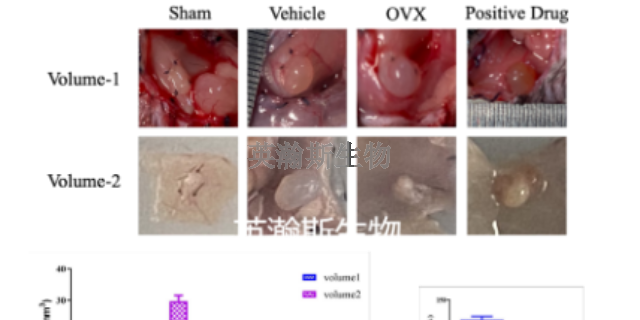
采用自体移植方法建立子宫内膜异位症大鼠模型,比较不同移植部位的建模效果。方法 取40只雌性、成熟未交配SD大鼠,将自体子宫内膜组织分别移植于卵巢、宫骶韧带及腹壁上,术后28 d手术取出移植物,测量移植物的体积和质量,对移植物进行组织形态学观察并比较不同部位的成模率。结果 卵巢部位移植物体积和质量大于其他两个部位(P<0.05),而宫骶韧带及腹壁部位的移植物体积及质量差异无统计学意义。3个不同部位的成模率差异无统计学意义,且移植物组织病理学相似。结论 卵巢、宫骶韧带及腹壁3个部位的自体子宫移植均可建立子宫内膜异位症模型,病理改变与子宫内膜异位症患者相似,但卵巢部位建模效果比较好,更有利于子宫内膜异位症新的治疗方法的开发及研究。该模型为我们揭示了子宫内膜异位症中细胞信号传导的异常变化。湖北大鼠子宫内膜异位症模型
研究人员正在利用子宫内膜异位症模型开发个性化的改善方案。江苏专业的子宫内膜异位症模型实验外包
子宫内膜异位症(endometriosis,EM)是一种因子依赖性的常见良性变化,多发于生育年龄妇女,其发病率为10%-159毛。迄今为止,关于EM的真正发病机制并未比较终阐明,且缺少有效的治疗方法。其中一个主要原因是这种疾病只发生于人类和灵长类动物。由于实际操作和伦理学方面的约束,严重限制了对该疾病的研究,因此需要一种可在实验动物体内复制该病的方法。1922年Jacobson初次建立了兔的EM模型,从而开创了EM研究的新局面。本文就EM模型建立、应用的现状及进展进行综述。江苏专业的子宫内膜异位症模型实验外包