肺纤维化模型在医学研究中扮演着至关重要的角色,它不仅是科学家们深入探索肺部纤维性疾病机理的桥梁,更是推动疾病疗愈方法创新的关键工具。通过构建和模拟肺纤维化的病理过程,这个模型能够重现肺部组织从炎症到纤维化的转变,使研究人员能够直观地观察到疾病发展的每一个阶段。肺纤维化模型不仅能够帮助我们理解疾病的具体机制,还能为评估疗愈策略的有效性提供可靠的实验平台,从而推动肺纤维化疾病疗愈领域的进步,为患者带来更多的希望和福音。肺纤维化模型为研究疾病过程中的微生物组变化提供了平台。云南比较好的肺纤维化模型如何构建
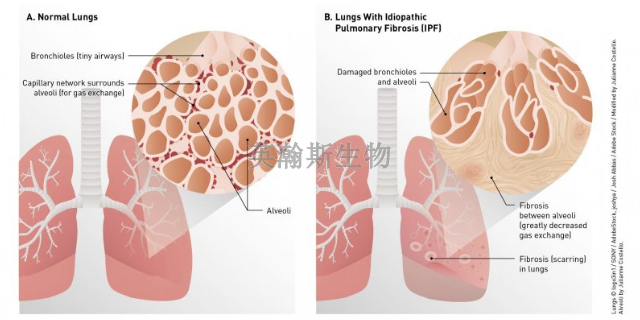
博莱霉素诱导的肺纤维化动物模型是广泛应用于肺纤维化研究的模型之一,目前世界上普遍采用博莱霉素的大鼠双侧肺模型和小鼠双侧肺模型,建模方法多使用博莱霉素滴鼻建立,由于肺组织有多叶的生理结构,此两种模型均有病变分布不均匀的情况,同时建模期间死亡率较高。本试验采用博菜霉素诱导大鼠的单侧肺纤维化动物模型,改变双侧模型中病变分布不均匀的现象,同时降低建模期间的动物死亡率,提高了成功率和动物存活率,该模型能真实模拟肺纤维化的病理过程,模型成功率高,稳定性好,死亡率低。云南比较好的肺纤维化模型如何构建科学家通过肺纤维化模型发现了一些与疾病相关的微小RNA。
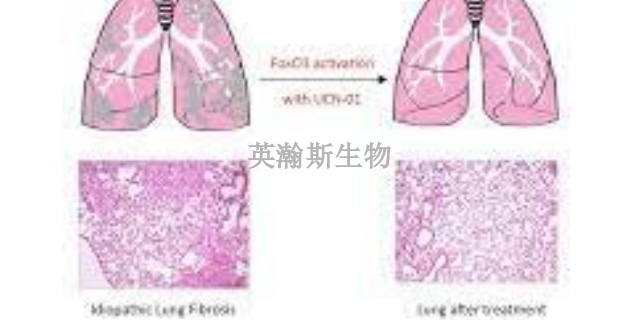
肺纤维化模型的并发症可能包括:肺部***(肺高压)。不同于全身性***,这种疾病只会影响肺部动脉。当瘢痕组织挤压比较细小的动脉和***时,会增加肺部血流阻力,从而导致这种疾病。这转而增加了肺动脉和右下心腔(右心室)内的压力。某些类型的肺高压是严重疾病,会逐渐恶化,有时甚至会致命。右心衰竭(肺源性心脏病)。当心脏右下心腔(心室)必须比平时更用力地泵送血液才能通过部分阻塞的肺动脉时,就会发生这种严重疾病。呼吸衰竭。这往往是慢性肺病的***阶段。当血氧水平下降至危险低水平时就会发生这种情况。肺*。长期肺纤维化也会增加您患肺*的风险。肺部并发症。随着肺纤维化恶化,可能会导致肺部血凝块、肺萎陷或肺部***等并发症。
肺纤维化模型发展时间:给药后第 7 天肺组织大多呈重度肺泡炎改变,肺泡腔及肺间质内有大量中性粒细胞浸润,部分肺泡腔破坏或消失,肺间隔内成纤维细胞和***增生,与正常肺组织对比差别明显;给药后第14天,肺纤维化开始形成。巨噬细胞、中性粒细胞等炎性细胞明显减少,成纤维细胞增多,肺泡间隔明显增厚,有胶原沉积。给药后第28天,多数小鼠发生弥漫性肺间质纤维化,肺间质被胶原纤维和成纤维细胞替代,肺泡壁破坏,肺大泡形成,但仍可见炎性细胞浸润。肺纤维化模型为研究疾病过程中的细胞凋亡和自噬提供了平台。
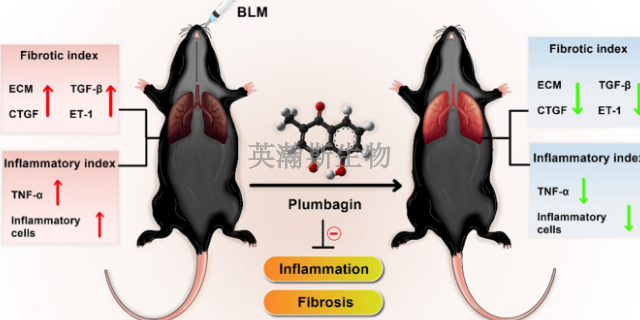
许多物质和疾病都可以导致肺纤维化。即便如此,在很多情况下无法找到具体原因。不明原因的肺纤维化叫做特发性肺纤维化。研究人员对引发特发性肺纤维化的原因有几种理论,包括病毒和接触***烟雾。此外,一些形式的特发性肺纤维化在家族中遗传,遗传可能在特发性肺纤维化中发挥作用。许多特发性肺纤维化患者也可能患有胃食管反流病(GERD)—一种胃酸流回食管的疾病。目前已有研究在评估GERD是否可能是导致特发性肺纤维化的风险因素,或者GERD是否可能导致病情进展更快。但还需要开展更多的研究来确定特发性肺纤维化与GERD之间的联系。肺纤维化模型为研究肺纤维化的表观遗传学机制提供了便利。河北真实的肺纤维化模型实验外包
肺纤维化模型为研究肺纤维化与其他肺部疾病的关系提供了帮助。云南比较好的肺纤维化模型如何构建
肺纤维化模型不仅模拟了肺纤维化的病理过程,更深入地揭示了疾病发展过程中细胞间相互作用的变化。在这个模型中,多种细胞类型如上皮细胞、成纤维细胞、免疫细胞等共同参与,并形成了复杂的细胞网络。随着疾病的进展,这些细胞间的相互作用会发生明显变化。例如,上皮细胞受损后可能释放炎症介质,刺激成纤维细胞增殖并产生过多的胶原蛋白,形成纤维组织。同时,免疫细胞的激发和迁移也会影响炎症反应的强度和持续时间。这些细胞间相互作用的变化不仅推动了肺纤维化的进展,也影响了疾病的临床表现和疗愈效果。因此,通过肺纤维化模型,研究人员可以更普遍地了解细胞间相互作用的机制,为疾病的疗愈提供新的思路和方法。云南比较好的肺纤维化模型如何构建