肺纤维化模型发展时间:给药后第 7 天肺组织大多呈重度肺泡炎改变,肺泡腔及肺间质内有大量中性粒细胞浸润,部分肺泡腔破坏或消失,肺间隔内成纤维细胞和***增生,与正常肺组织对比差别明显;给药后第14天,肺纤维化开始形成。巨噬细胞、中性粒细胞等炎性细胞明显减少,成纤维细胞增多,肺泡间隔明显增厚,有胶原沉积。给药后第28天,多数小鼠发生弥漫性肺间质纤维化,肺间质被胶原纤维和成纤维细胞替代,肺泡壁破坏,肺大泡形成,但仍可见炎性细胞浸润。肺纤维化模型有助于理解肺纤维化与吸烟和其他肺部刺激物之间的关系。辽宁大鼠肺纤维化模型如何构建

肺纤维化模型在医学研究中展现出了其独特的价值,特别是在揭示肺纤维化与心血管疾病之间复杂关系方面。通过精心构建的肺纤维化模型,科学家们能够模拟出与真实患者相似的病理生理状态,进而深入探索肺纤维化对心血管系统可能产生的潜在影响。这种模型不仅为我们提供了一个观察和研究两者相互作用的平台,还为我们揭示了它们之间可能存在的共同病理机制和风险因素。这些线索不仅有助于我们更普遍地理解肺纤维化和心血管疾病的发病机制,还可能为开发针对这两种疾病的联合治疗方法提供新的思路。甘肃靠谱的肺纤维化模型实验外包通过肺纤维化模型,科学家可以评估不同治疗方法的长期效果。
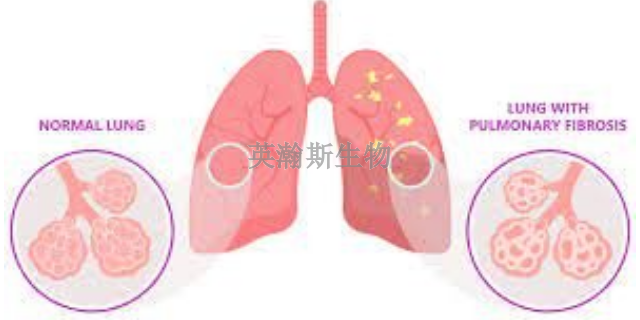
在肺纤维化的研究中,肺纤维化模型为我们揭示了免疫细胞异常激发对疾病发展的重点影响。当肺部受到外界刺激或损伤时,免疫细胞如巨噬细胞、T淋巴细胞等会被异常激发,释放出一系列炎症介质和细胞因子。这些介质和因子在促进炎症反应的同时,也加剧了肺组织的损伤,并启动了纤维化的进程。在肺纤维化模型中,研究人员观察到免疫细胞的异常激发与肺纤维化的发生和进展密切相关。这种异常激发状态不仅导致了肺组织的持续炎症,还促进了纤维细胞的增殖和胶原蛋白的过度沉积,从而加速了肺纤维化的形成。因此,理解并调控免疫细胞的异常激发对于肺纤维化的疗愈具有重要意义。
在肺纤维化模型的研究中,科学家们发现了一个关键的因素:肺纤维化的发展与氧化应激和抗氧化防御系统之间的失衡紧密相关。氧化应激是指机体内活性氧自由基的过量产生,而抗氧化防御系统则负责去除这些有害的自由基,保护细胞和组织免受损伤。在肺纤维化模型中,当肺部受到外界刺激或损伤时,氧化应激水平会明显升高,而抗氧化防御系统的功能可能受损,导致两者之间的平衡被打破。这种失衡状态加剧了肺组织的氧化损伤,促进了肺纤维化的进展。因此,了解并调节氧化应激与抗氧化防御系统之间的平衡,对于预防和疗愈肺纤维化具有重要意义。肺纤维化模型揭示了疾病过程中炎症介质的作用。
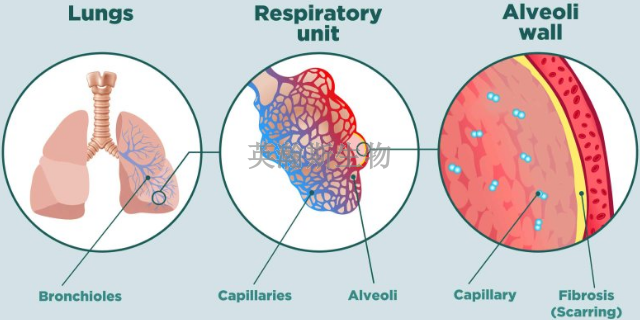
肺纤维化形成***组织。***一旦形成,便是长久性的。基于疾病的不同,可采取如下方式延缓疾病进展,开展预防:特发性肺纤维化的疗愈选择非常有限。尽管研究试验仍在进行,目前为止没有证据表明任何药物可以明显改善病情。重症病例单独可能的疗愈选择是肺移植。某些类型的肺纤维化对皮质类固醇(如泼尼松)及其他免疫抑制药物产生反应,因此有时会使用这些药物减缓纤维化过程。免疫系统在多种肺纤维化的发展中发挥着中心作用。使用免疫抑制剂(如皮质类固醇)的目的是减少肺部炎症和伴随的瘢痕形成。病情对药物疗愈的反应不尽相同。免疫抑制疗愈有效的患者或许并非患有特发性肺纤维化,特发性肺纤维化尚无明确的疗愈方法。科学家通过肺纤维化模型发现了一些新的疾病疗愈靶点。河南肺纤维化模型如何构建
在肺纤维化模型中,胶原蛋白的过度沉积是肺纤维化的一个重要特征。辽宁大鼠肺纤维化模型如何构建
间质性肺疾病(ILD)的病理改变可严重影响肺泡上皮细胞和血管内皮细胞功能及气体交换,病程终末期会出现呼吸衰竭,目前尚无明确有效的疗愈方法。对博莱霉素致小鼠肺纤维化发生不同阶段的肺组织病理、肺组织中不同细胞因子的表达以及外周血T细胞亚型进行研究,以探讨肺纤维化在ILD不同阶段的发生机制,从而为临床制定有效的疗愈策略提供理论和实验依据。给予博莱霉素后小鼠表现为炎症反应,早期为急性中性粒细胞浸润,随后过渡为淋巴细胞增多的慢性表现,与Izbicki等“的研究结果一致。Tarnell等的研究指出,纤维化模型BALF中中性粒细胞比血液中中性粒细胞产生更多的超氧阴离子。辽宁大鼠肺纤维化模型如何构建