- 品牌
- 有梦生物
- 服务项目
- 切片染色
分化与返蓝是HE染色中调节细胞核显色的关键步骤,其操作精度直接影响染色质量和诊断准确性。分化过程使用1%盐酸乙醇溶液(通常由1ml浓盐酸与99ml 70%乙醇配制),其主要作用是选择性去除细胞质中非特异性结合的苏木精染料,同时保留细胞核内的强结合染料,从而增强核质对比度。实际操作中需严格控制分化时间(通常5-30秒),并在显微镜下动态观察,以细胞核结构清晰可见而细胞质基本无色为比较好终点。分化不足会导致背景过深,细胞核与细胞质界限模糊;分化过度则可能使细胞核染色过浅,丢失重要诊断信息。
巴氏染色常用于宫颈细胞学检查,通过显示核染色质细节帮助筛查宫颈上皮内瘤变及早期宫颈。北京肠病理切片

纳米染色技术****前沿发展方向:量子点标记:CdSe/ZnS量子点(发射峰可调)的荧光强度是传统FITC的20倍,特别适用于低表达抗原(如EGFR突变体)表面增强拉曼(SERS):金纳米颗粒标记抗体后,通过特征拉曼位移可同时识别10种以上生物标志物数字PCR整合:微流控芯片上的纳米级反应室可实现单细胞水平mRNA原位检测这些技术在临床转化中已显现巨大价值:**早诊:CytoPAN平台通过纳米抗体染色可在2小时内完成乳腺*穿刺标本的5标志物快速诊断用药指导:NGS联合mIHC可预测PD-1抑制剂疗效(如CD8+Tex细胞空间分布模式)预后评估:AI算法通过H&E染色图像可预测结直肠*微卫星不稳定性(AUC=0.92)河北脾病理切片24小时服务刚果红染色在淀粉样变性诊断中具有特异性,偏振光下呈现苹果绿双折光可作为确诊的重要依据。
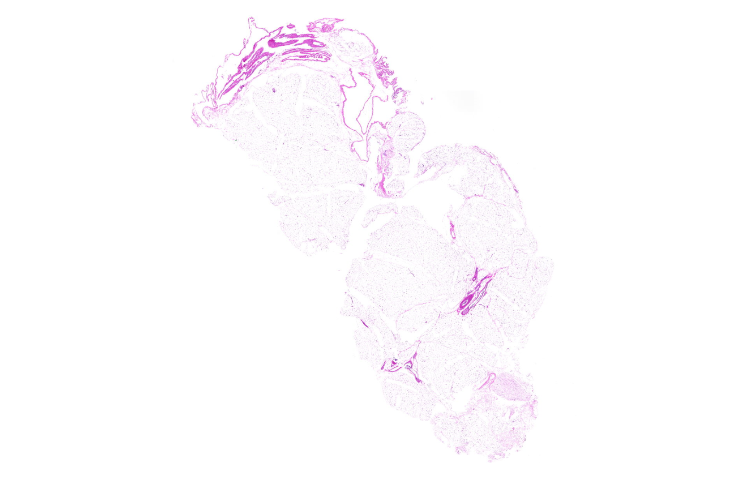
近年来,随着分子病理学和人工智能技术的深度融合,病理切片染色技术正经历**性变革。多重免疫荧光染色(mIHC/mIF)通过光谱分离技术(如Opal 7色系统)可在单张切片上同步检测PD-L1/CD8/FOXP3等7种标志物,结合多光谱成像系统(如Vectra Polaris)实现**微环境免疫细胞亚群的精确定量,其空间分辨率可达0.25μm/pixel,较传统IHC诊断效率提升5倍以上。数字病理与AI分析已进入临床实用阶段,如谷歌DeepMind开发的乳腺*淋巴结转移检测系统(灵敏度达99.3%),可对全切片图像(WSI)进行实时分析,自动标注可疑区域并生成结构化报告。
数字化病理技术的快速发展为组织染色质量的客观评估提供了高效、标准化的解决方案。借助专业图像分析软件(如Aperio ImageScope、HALO等),研究人员能够对染色切片进行自动化定量评估,大幅提升分析效率和准确性。这些软件系统通常采用多维度的评估指标:核质对比度通过计算苏木素(细胞核)和伊红(细胞质)的灰度值差异来量化染**分度;染色均匀性则利用统计学方法(如像素强度的标准差分析)评估整张切片的染色一致性;阳性信号面积比例通过智能阈值分割技术精确识别目标染**域(如免疫组化的棕褐色阳性信号),并计算其占组织总面积的比例;背景噪声水平则采用信噪比分析来鉴别有效信号与非特异性染色。相较于传统人工评估,自动化分析不仅避免了主观偏差,还能同时处理大批量切片数据,显著提高筛查效率。此外,数字化评估可生成标准化报告,便于不同实验室间的数据比对和质量控制,为精细医学研究和临床病理诊断提供可靠的技术支持。组织化学染色与质谱联用技术,能在保留形态学信息的同时获取分子组成的高通量数据。
苏木精染色的时间会直接影响细胞核的显色效果。如果染色时间不足,细胞核可能会呈现灰蓝色,导致核结构模糊;如果染色时间过长,细胞核会过度吸收染料,呈现深紫色,甚至会掩盖核内细节。在实际操作中,需根据组织类型和切片厚度调整染色时间,通常为5-15分钟。染色后需用1%盐酸乙醇分化,去除多余染料,再通过温水或自来水冲洗返蓝,使细胞核呈现清晰的蓝紫色。分化时间需在显微镜下控制,以细胞核染色清楚而细胞质基本无色为佳。黑色素染色如Fontana-Masson法能显示无色素性黑色素瘤中的前黑素颗粒,避免漏诊风险。脑组织病理切片售后服务
磷钨酸苏木精(PTAH)染色可显示横纹肌的横纹结构,在心肌病变或横纹肌肉瘤诊断中具有特异性。北京肠病理切片
该染色法的诊断价值主要体现在对组织纤维化的评估上:在肝硬化标本中,可清晰显示门静脉区增生的蓝色胶原纤维包绕红色肝细胞团;在肺纤维化组织,能明确区分肺泡间隔内异常沉积的蓝色胶原纤维与正常肺间质结构;在心肌梗死后修复过程中,可准确识别红色存活心肌与蓝色瘢痕组织的界限。此外,Masson染色还能帮助鉴别**间质反应程度,如浸润性乳腺*中可见*细胞巢被蓝色胶原纤维包绕,而平滑肌肉瘤则表现为弥漫的红色肌源性分化区域。现代数字化病理分析系统常基于Masson染色结果进行胶原面积定量,为纤维化疾病的疗效评估提供客观指标。该技术因其稳定的染色效果和明确的组织对比度,至今仍是结缔组织病理诊断的基石性方法。北京肠病理切片
- 大鼠病理切片销售电话 2026-04-03
- 天津肠病理切片销售电话 2026-04-03
- 江苏肠病理切片销售 2026-04-03
- 四川脑组织病理切片销售价格 2026-04-03
- 广东心脏病理切片电话多少 2026-04-03
- 陕西肝脏病理切片电话多少 2026-04-03
- 云南肠病理切片 2026-04-02
- 宁夏肠病理切片 2026-04-02
- 广东血管病理切片电话多少 2026-04-02
- 甘肃脾病理切片销售价格 2026-04-02
- 湖南大鼠病理切片实验效果 2026-04-02
- 甘肃脑组织病理切片服务电话 2026-04-02